
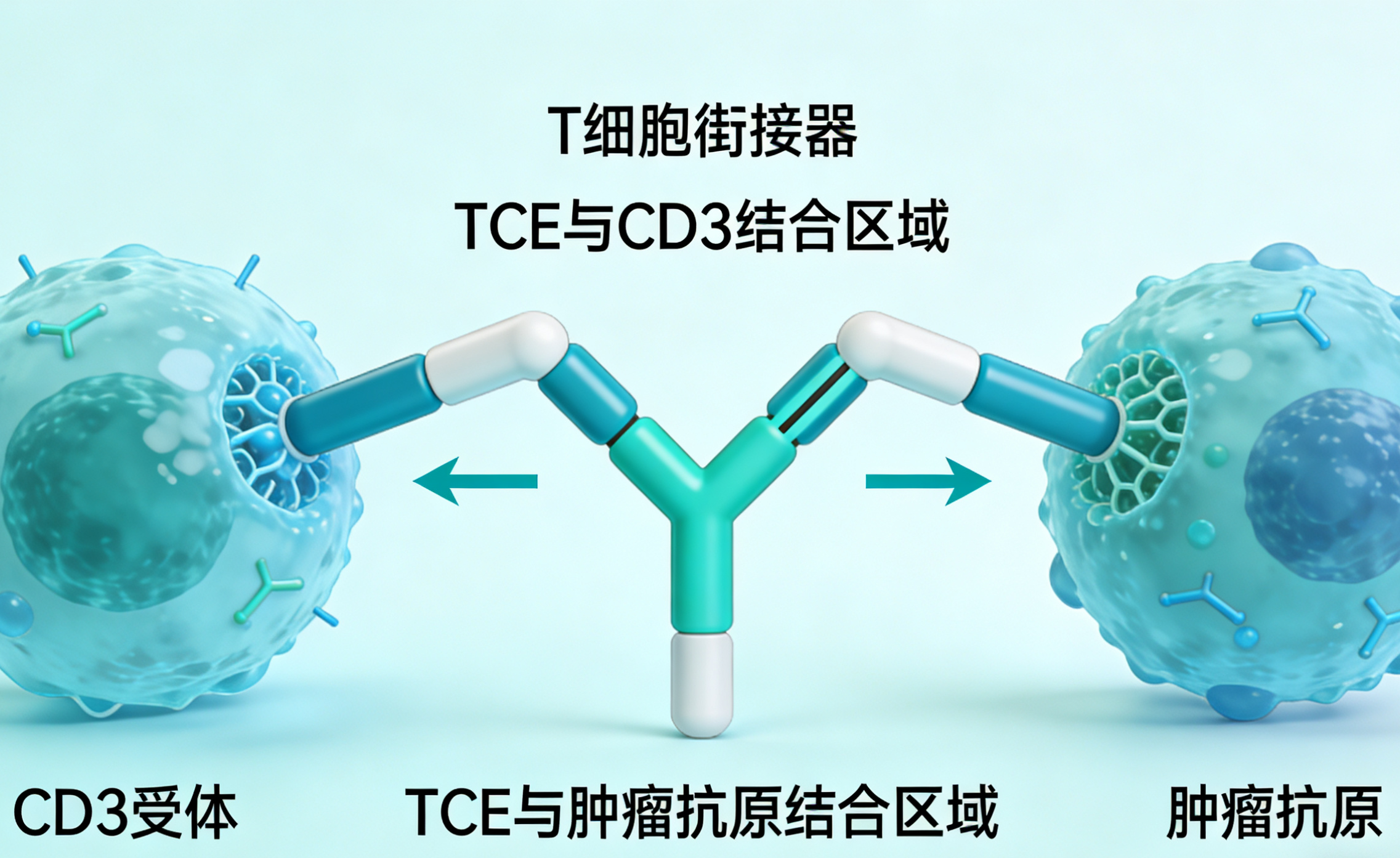
千靶万抗:2025-2026 AACR 一年跨越,靶点迭代!
血液瘤与实体瘤双轮驱动:血液瘤:BCMA、CD20、GPRC5D 、CD19等成熟靶点占据(T细胞衔接器)TCE赛道半壁江山,三抗、四抗技术平台迭代加速更新,临床转化速度领跑;实体瘤:DLL3、CLDN6、Nectin-4 、B7-H3等免疫靶点快速崛起,双抗ADC成为主流技术形态,突破实体瘤治疗瓶颈。2、老靶点,新应用,迭代焕新:EGFR、HER2、TROP2 、PD-1/PD-L1、HER3等经典老靶点通过双抗 /双抗ADC形式再次回到大众视野,重点解决靶点选择、连接子稳定性、耐药、肿瘤微环境免疫调节等未满足的临床需求,赛道虽卷,但是很火。
了解详情
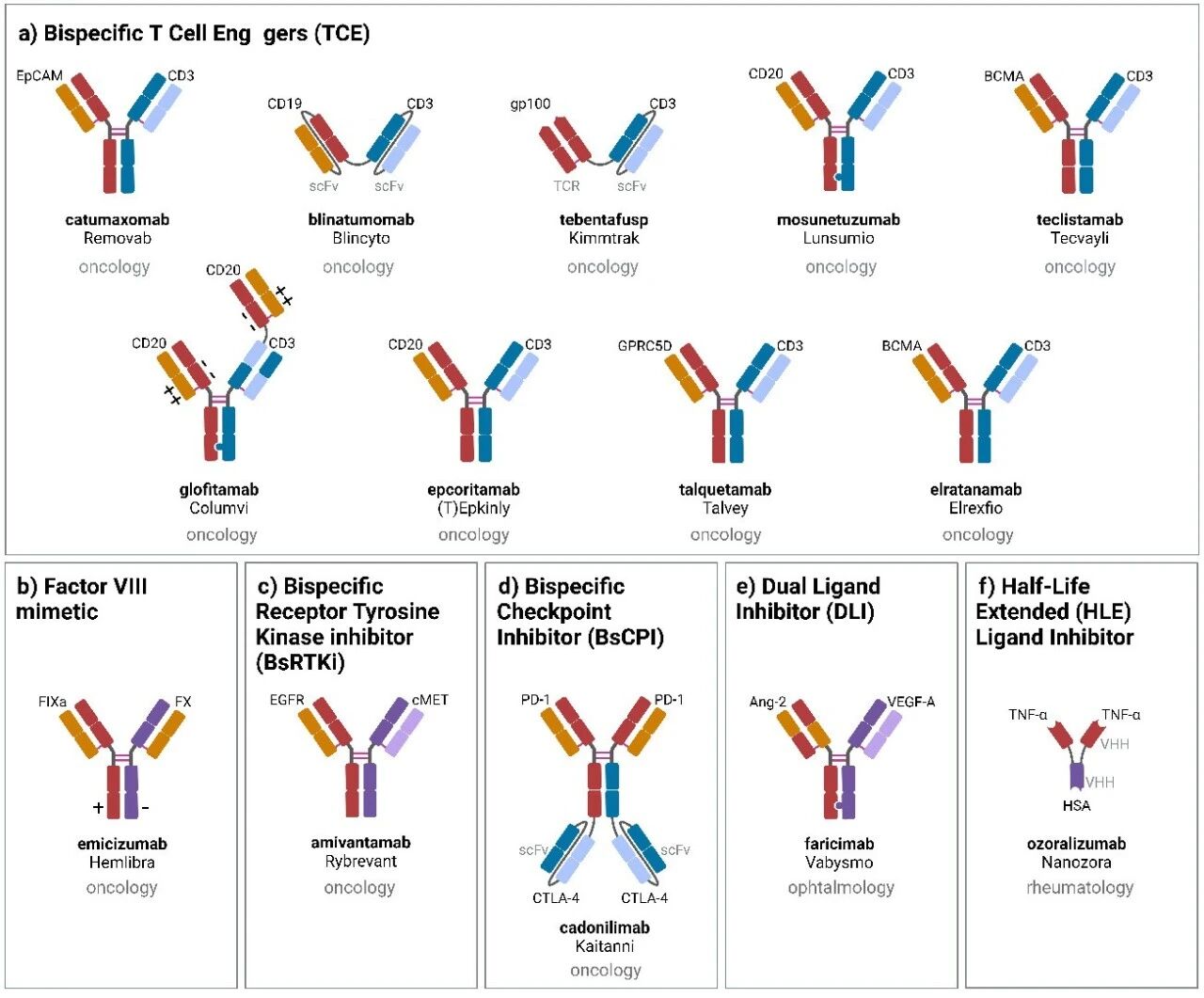
千靶万抗:双特异性抗体的关键十年?
双特异性抗体(bispecific antibodies, bsAbs)是一类相较单特异性单克隆抗体(monoclonal antibodies, mAbs)可介导全新作用机制的抗体药物。自 20 世纪 80-90 年代单克隆抗体被发现并应用于治疗领域以来,双特异性抗体的研发始终具备极高的行业关注度。但截至 2020 年底,全球仅 3 款双特异性抗体(卡妥索单抗、博纳吐单抗、艾美赛珠单抗)获批上市。2021 年至今,已有 11 款双特异性抗体获得监管机构批准,其中 9 款(埃万妥单抗、替本福司、莫舒妥珠单抗、卡度尼利单抗、特立妥单抗、格菲妥单抗、埃普妥珠单抗、塔奎妥单抗、埃兰妥单抗)获批用于肿瘤治疗,2 款(法瑞西单抗、奥佐利珠单抗)获批用于非肿瘤适应症。值得关注的是,目前获批的 13 款双特异性抗体中,艾美赛珠单抗与法瑞西单抗已达成重磅炸弹级销售业绩,充分印证了这一新型治疗药物的发展潜力。2020-2030 年,血液系统恶性肿瘤、实体瘤及非肿瘤适应症领域将迎来更多双特异性抗体获批,该类药物将成为临床治疗体系中的核心组成部分。
了解详情

2026年全球双特异性抗体和纳米抗体发现CRO行业分析
双特异性抗体和纳米抗体发现CRO行业作为生物医药研发外包服务的重要分支,正处于快速发展的黄-金期。双特异性抗体(Bispecific Antibodies, BsAb)是一类能够同时结合两个不同抗原或同一抗原两个不同表位的抗体分子,通过协同靶向机制在-肿瘤治疗、自身免疫疾病等领域展现出独特优势。纳米抗体(Nanobodies)则是源自骆驼科动物重链抗体的单域抗体,具有分子量小、稳定性高、组织穿透性强等特点,在诊断、治疗和研究领域应用广泛。
了解详情
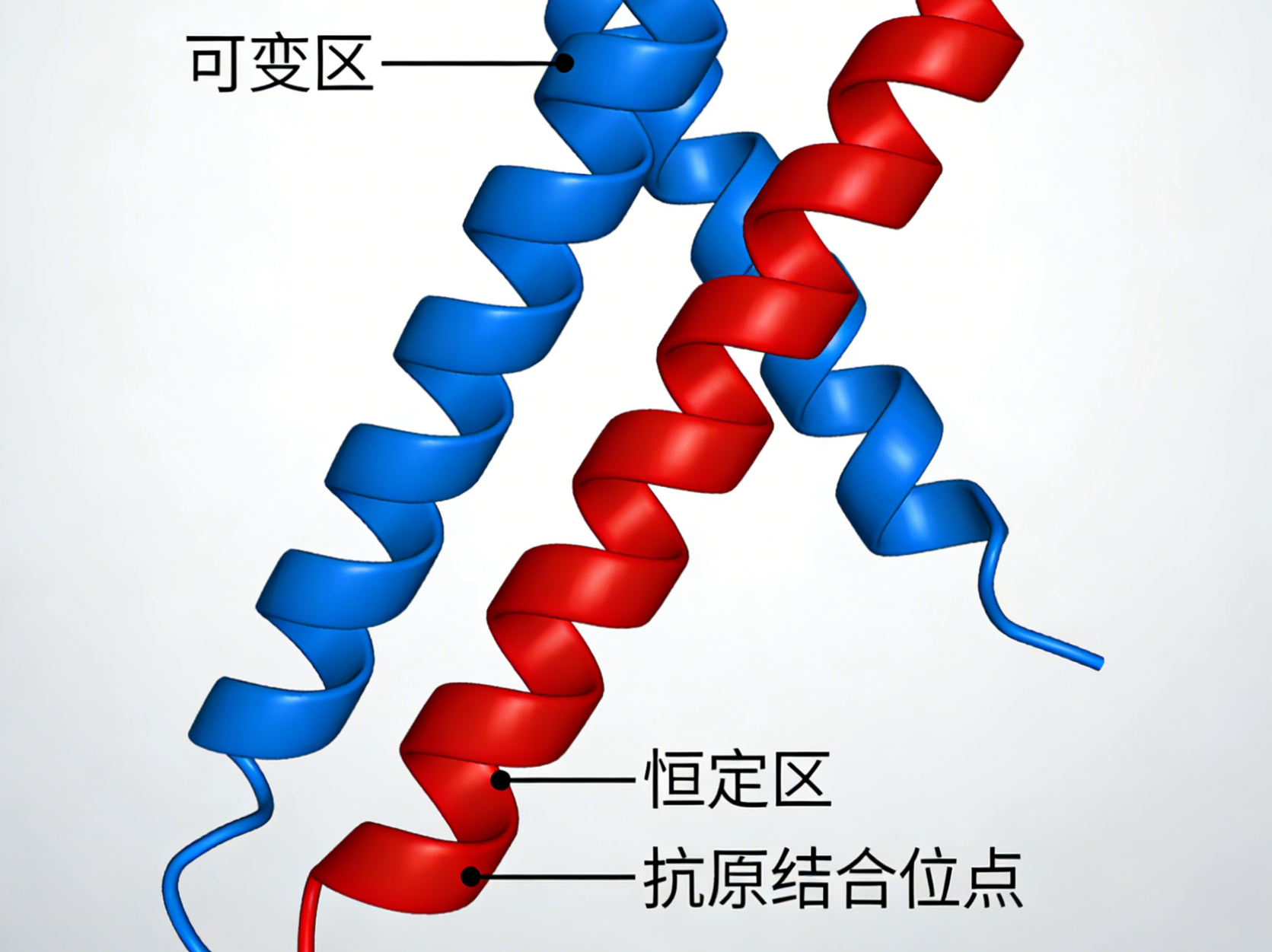
从发现到临床:详细了解骆驼源纳米抗体VHH!
骆驼科单域抗体(VHH)是构建药物候选分子的理想模块。截至2025年10月,全球已有5款VHH药物获批上市。VHH不仅具备与传统抗体相仿的亲和力与特异性,其独立结构还兼具分子量小、稳定性高的特点;且因无需轻链配对,更易于进行多格式工程化改造。本文综述了VHH的结构特征、物种间序列差异、以及其分离与人源化的平台技术;梳理了已上市VHH药物的构成与作用机制;并对49条进入临床的VHH序列进行了计算分析,为未来基于VHH的药物开发提供参考。
了解详情

千靶万抗:全人源纳米抗体VH抗聚集双特征:二硫键与酸性pI
本研究利用噬菌体展示技术与瞬时热变性筛选法,从一个预置CDR3二硫键的库中,成功富集到可逆折叠且抗聚集的VH。这些优质VH普遍具备两个关键结构特征:一是在CDR1与CDR3之间或内部形成了非经典的二硫键;二是其理论等电点呈酸性(pI < 6)。这为优化人工单域抗体提供了两条明确思路:引入CDR区二硫键与降低等电点。相关名词有:二硫键环、等电点、抗聚集VH 、噬菌体展示和筛选、单域抗体。获得低免疫原性的全人源单域抗体,其核心挑战在于克服VH域的易聚集性。本研究富集到的优质VH均具备特征:CDR区二硫键与酸性等电点,与骆驼、鲨鱼天然单域抗体的进化策略一致。
了解详情
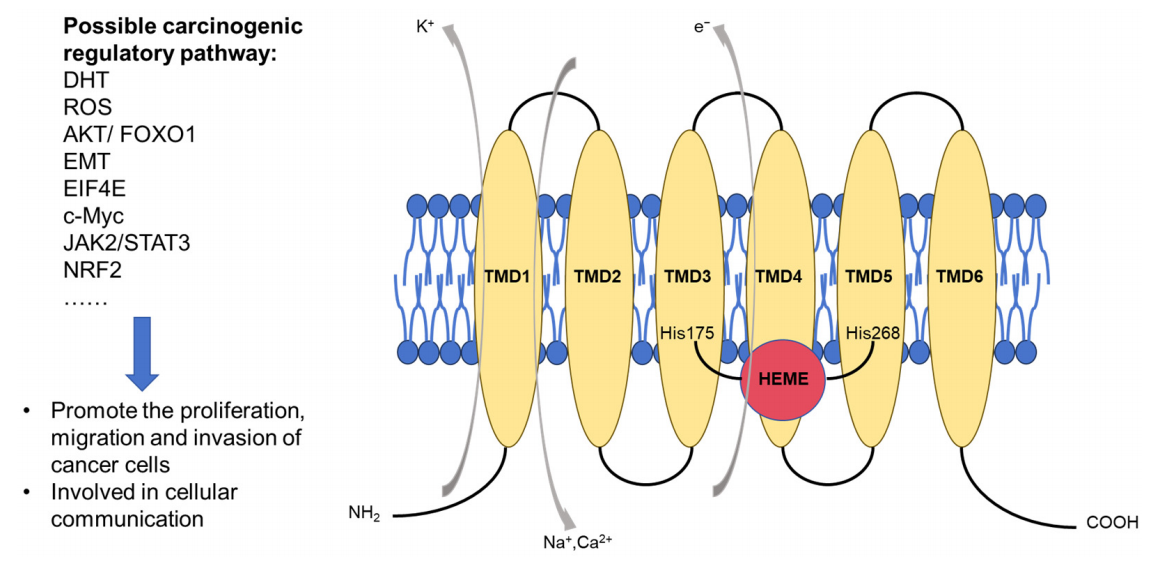
靶点STEAP1:在前列腺癌诊疗中的重要作用和进展!
六次跨膜前列腺上皮抗原1(STEAP1)是一种在PCa和mCRPC中持续高表达的理想靶点。然而,其复杂的多次跨膜结构曾让传统小分子与抗体药物难以有效靶向。近年来,得益于结构生物学及药物研发技术的进步,这一困境得以破局,针对STEAP1的多种创新疗法(如ADC、CAR-T、TCE和疫苗)正蓬勃发展,显示出广阔前景。
了解详情

自免的CAR-T治疗:In vivo与Ex vivo双轨并行!
体内CAR T技术(通过靶向脂质纳米颗粒或慢病毒载体直接体内改造T细胞)可能解决这些问题,但其在自身免疫病中的安全性与有效性尚不明确。研究采用的是MB-CART19.1,这是一种自体来源的、通过慢病毒转导在体外制备的CD19 CAR T细胞产品,还有采用HN2301,一种靶向CD8+T细胞的脂质纳米颗粒(LNP),其内部封装了可编码靶向CD19蛋白的CAR的mRNA。
了解详情
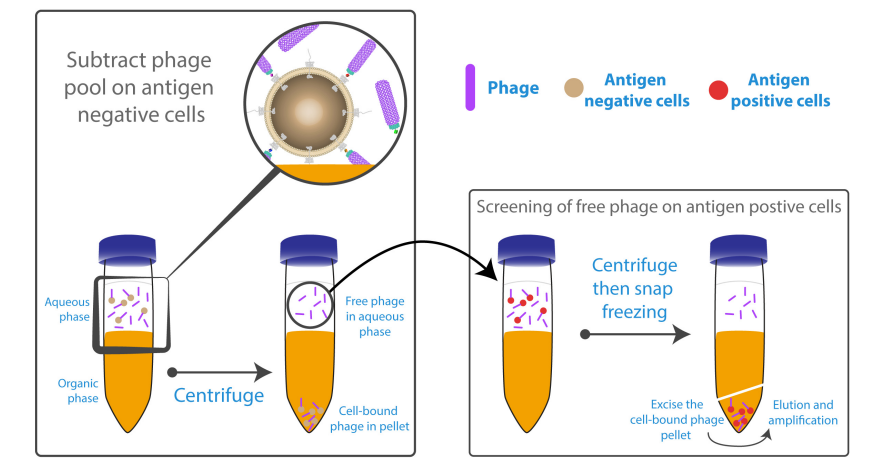
噬菌体展示技术:膜蛋白抗体的细胞筛选法!
膜蛋白(如GPCRs、离子通道)是关键治疗靶点,但其固有的疏水性与结构不稳定性使得传统基于纯化蛋白的筛选策略面临巨大挑战:纯化过程易导致蛋白变性、构象失真,从而筛选出无法识别天然表位的无效抗体。本研究采用基于完整细胞的筛选策略,保持膜蛋白天然构象和修饰,确保抗体功能相关性。预实验针对TLR2表明,传统策略无效,而细胞筛选成功分离出8个具天然活性的克隆,验证了平台有效性。
了解详情
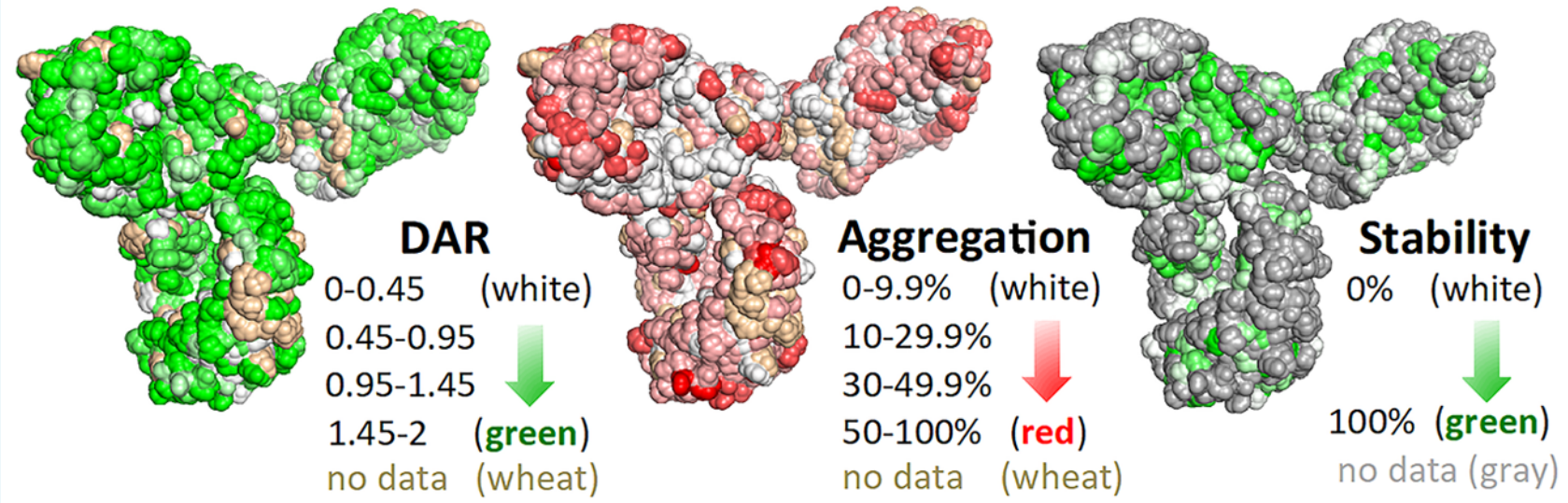
偶联的“命门”所在:如何让药物在抵达目标前不“掉链子”
本研究通过高通量半胱氨酸扫描,系统评估了曲妥珠单抗648个单点Cys突变体与两类ADC连接子(马来酰亚胺vs二硫键)的血浆稳定性。约50%的突变体实现高效偶联(DAR>0.5、聚集<50%),并锁定38个对两类连接子均>80%稳定的位点。结果证实:偶联位点决定连接稳定性,且该稳定性可跨抗体、跨载荷、跨物种保持一致。参考文献:High-Throughput Cysteine Scanning To Identify Stable Antibody Conjugation Sites for Maleimide- and Disulfide-Based Linkers.
了解详情

聚力研发,千靶万抗:成都古格尔生物2025年中团建活动圆满结束!
为增强团队凝聚力、缓解工作压力,感谢大家一直以来的辛苦付出和努力拼搏,成都古格尔生物于2025年08月19日-22日组织了“聚力研发,千靶万抗”主题团建活动,公司全体成员参与。此次团建不仅让大家在户外放松了身心,更重要的是强化了“目标一致、彼此信任,聚力研发”的团队意识。活动后,成员们通过团队协作更直观地感受到了沟通与配合的重要性,未来将把这种团队精神融入工作,提升公司整体效率。
了解详情